医疗器械唯一标识(UDI)作为全球医疗器械管理的“数字身份证”,通过唯一编码实现从生产到使用的全生命周期追踪。然而,UDI系统的有效运行离不开严格的监管机制,这既是保障患者安全的底线,也是提升行业效率的必然要求。

监管是UDI追溯的“安全阀”
UDI的核心价值在于快速定位问题产品。例如,当某批次人工关节出现质量问题时,医疗机构可通过扫描UDI码在数秒内锁定同批次所有产品,监管部门则能通过数据库追溯其生产、流通路径,实现精准召回。但若缺乏监管,企业可能因成本考虑简化追溯流程,导致关键信息缺失。我国《医疗器械管理法(草案)》明确要求企业建立追溯制度,未按规定执行的将面临罚款甚至吊销许可证的处罚,这正是通过法律强制力确保UDI数据完整性的关键举措。
监管推动UDI与产业生态深度融合
监管不仅规范企业行为,更通过标准化建设打破数据壁垒。湖南省推行的“三码融合”机制(医保编码、追溯码、商品码)和“一码贯通”全流程,正是监管部门主导的典型实践。通过统一编码标准,监管部门要求医疗机构、经营企业、生产企业必须实时上传UDI数据至省级平台,实现“带码交易、带码结算”。这种跨部门协作模式,使UDI从单一标识升级为全链条管理工具,既方便患者查询产品真伪,又为医保控费、招标采购提供数据支撑。
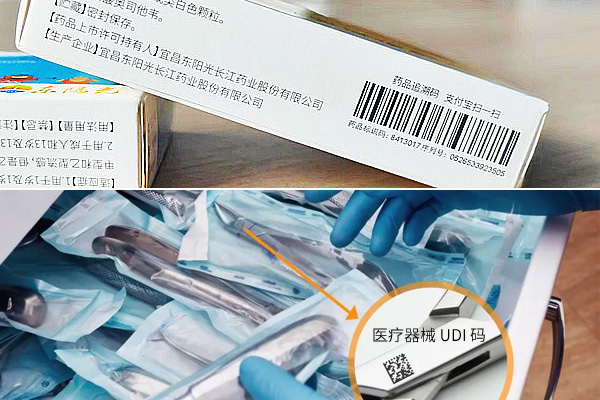
UDI追溯码扫码设备
如销邦SK9028C,采用激光扫描技术,可连续扫描多码,设备内置Android 13操作系统,高性能八核处理器,配备4+64GB存储空间,支持药品企业APP与医疗机构物资管理系统无缝对接。此类双码兼容型PDA扫码枪通过技术融合打破数据孤岛,推动药品与医疗器械追溯体系向集成化、智能化演进,为医疗供应链数字化转型提供关键支撑。

UDI器械码追溯的本质是“用数据说话”,而监管则是确保数据真实、完整、可用的“守护神”。只有构建“法规强制+技术支撑+协同共治”的监管体系,才能让UDI真正成为保障医疗安全、推动行业高质量发展的“数字引擎”。













